Neural Regeneration Research | RNA m6A参与调控视网膜星形胶质细胞的发育性死亡和视网膜血管的维持
中枢神经系统中的星形胶质细胞参与维持了多种结构和功能,其中视网膜星形胶质细胞在视网膜血管发生、重塑和退化的过程中都起着重要的调控作用。许多视网膜疾病如家族性渗出性玻璃体视网膜病变、高血压性视网膜病变等,病程中发生的视网膜微血管或病理性血管的异常重塑最终很可能导致不可逆的视觉损伤。而大量报道证明在这些病理情况下的微血管失调还同时伴随着星形胶质细胞的病理性变化。而近期,m6A被报道广泛参与了中枢神经系统发育和多种神经退行性疾病 其中已有研究证明m6A能够调控视网膜祖细胞的细胞周期和分化命运、视网膜神经元的存活等,但关于m6A在视网膜星形胶质细胞及其介导的神经血管串扰的调控功能和机制仍不清楚。
2026年1月27日,深圳理工大学周涛团队在《中国神经再生研究(英文版)》(Neural Regeneration Research)上发表了题为“The m6A writer VIRMA regulates the developmental elimination of retinal astrocytes and retinal vascular integrity maintenance”的研究论文。研究发现在视网膜星形胶质细胞中条件性敲除m6A甲基转移酶复合物的核心支架蛋白VIRMA会影响出生后视网膜星形胶质细胞的发育性死亡过程,该过程是通过小胶质细胞吞噬介导的;这种异常的星形胶质细胞积累会进一步影响视网膜血管的维持功能和小鼠视觉功能。该文确定了VIRMA/m6A作为一种新型的调控分子,可能能作为视网膜病变治疗的潜在靶点。
N6-甲基腺嘌呤(m6A)修饰是真核生物中广泛存在的转录后调控机制,其由甲基转移酶复合物(m6A writer,包括METTl3、METTL14、WTAP和VIRMA等)和去甲基化酶(m6A eraser)共同调控实现在RNA上动态可逆的加/去甲基,并被m6A识别蛋白结合并发挥不同的功能进而影响RNA代谢和命运。VIRMA作为甲基转移酶复合物中组分最大的支架蛋白,在组装成完整的甲基转移酶复合物中发挥重要的作用。前不久,周涛团队报道VIRMA通过调控核糖体生成从而影响前脑发育的分子机制,也进一步揭示了VIRMA在中枢神经系统中的重要调控作用。但目前关于VIRMA及m6A在不同神经细胞类型,如神经元、胶质细胞中的功能仍不清晰。因此,该研究从中枢神经系统的星形胶质细胞入手,通过构建条件性敲除小鼠探究VIRMA介导的m6A在视网膜星形胶质细胞中的重要调控功能。
视网膜星形胶质细胞在小鼠刚出生早期(约P0-P5)会从视神经头处往视网膜边缘迁移和增殖,此时视网膜星形胶质细胞数量达到峰值。随后(P5-P14),这些未成熟的星形胶质细胞会被小胶质细胞识别并吞噬,这个过程是视网膜星形胶质细胞的发育性死亡,剩下的星形胶质细胞趋于成熟且数量也维持稳定(图2a)。但是,研究人员发现VIRMA在视网膜星形胶质细胞中的特异性敲除会导致出生后早期(P9开始)的视网膜星形胶质细胞异常积累(图1),这是由于视网膜小胶质细胞的吞噬事件减少导致的(图2b-c)。
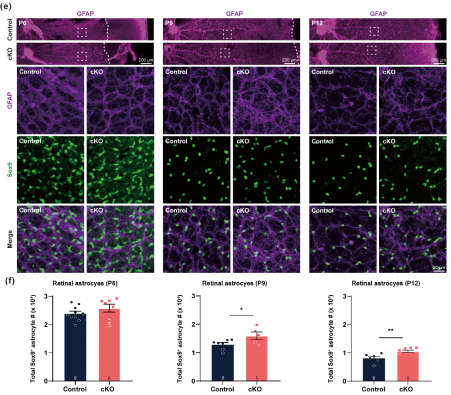
图1 VIRMA特异性敲除的视网膜星形胶质细胞数量从P9开始出现异常增多
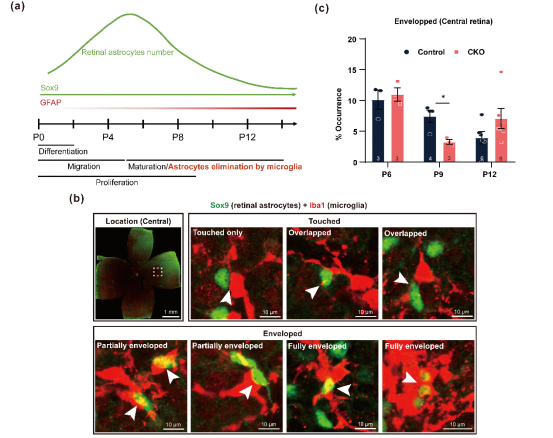
图2 视网膜星形胶质细胞中VIRMA缺失减少了P9小胶质细胞吞噬介导的星形胶质细胞消亡
随后,研究人员进一步发现视网膜星形胶质细胞中VIRMA缺失后会导致P30后的视网膜表层血管分支密度减少(图3)。此前有研究报道,产后视网膜的三层血管(表层、中间层和深层)在P17时就已经发育完成 。这说明星形胶质细胞的VIRMA并不影响视网膜血管的发生过程,而是调控了出生后期(P30之后)视网膜血管完整性的维持功能。异常积累的视网膜星形胶质细胞加上异常的视网膜血管系统恶化了视网膜内稳态环境,进一步造成条件性敲除小鼠的视觉功能明显受损。
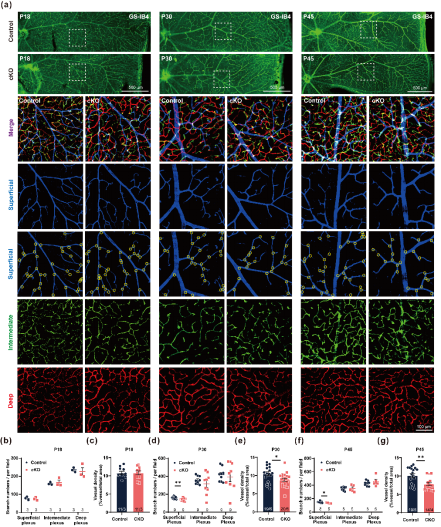
图3 VIRMA条件性敲除鼠的视网膜表层血管密度减少
为了探究VIRMA调控视网膜星形胶质细胞功能的分子机制,研究人员对条件敲除鼠和同窝对照的视网膜进行了单细胞核测序。对星形胶质细胞这一细胞群体分析发现:VIRMA可能通过调控细胞黏附、细胞外基质相关基因从而影响星形胶质细胞被小胶质细胞识别吞噬的过程。研究者进一步借助细胞通讯分析、MeRIP-qPCR等技术验证VIRMA可能通过m6A调控血管发生相关的基因(如Vegfa,Sema6a)来调控视网膜血管的维持功能(图4)。
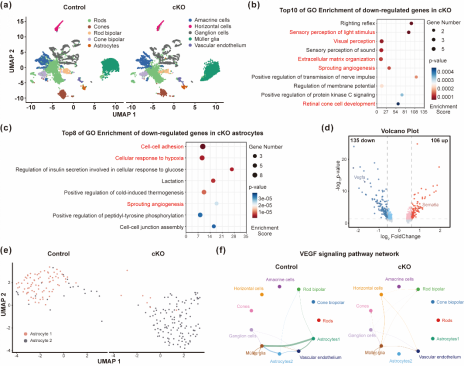
图4 VIRMA特异性敲除小鼠视网膜中与细胞间相互作用和血管生成相关的基因表达异常
综上所述,该研究阐明了VIRMA/m6A能够调控视网膜星形胶质细胞发育、视网膜血管的维持功能和视网膜内环境稳定(图5),为血管性视网膜病变提供了新潜在靶点。下一步研究将聚焦星形胶质细胞群体,构建其特异性m6A修饰图谱,精准解析m6A如何调控星形胶质细胞功能及其与周边细胞(如血管内皮细胞)的信号交流,进而开发视网膜血管疾病的新治疗策略。
深圳理工大学周涛副教授为该论文的通讯作者;深圳先进院博士生吴翠婷、博士后吴晓丽等为论文的共同第一作者。该研究在国家重点研发计划、广东省重点领域研发计划、国家自然科学基金、广东省基础与应用基础研究基金、深圳市基础研究专项自然科学基金计划和深圳市科技创新计划等经费的资助下完成。